Niedawne badanie preprint rzuciło światło na to, dlaczego zaobserwowano zdarzenia niepożądane po szczepieniu informacyjnego RNA COVID-19 (mRNA).
Badanie, prowadzone przez naukowców z Thomas Jefferson University, wykazało, że nanocząsteczki lipidowe (LNP) używane do transportu mRNA w szczepionkach COVID-19 mogą "hamować" i "zmieniać" odpowiedzi immunologiczne u myszy.
LNP to powłoki lipidów, które otaczają mRNA, aby zapobiec degradacji i wykrywaniu przez układ odpornościowy naszego organizmu.
LNP nie są mRNA, po prostu otoczką do transportu ładunku mRNA.
Zarówno szczepionki Pfizer, jak i Moderna mRNA COVID-19 wykorzystują konwertery do dostarczania sekwencji białek mRNA do komórek ludzkich. Gdy komórki ludzkie otrzymają sekwencje mRNA, komórki będą wytwarzać białka kolców, wywołując odpowiedź immunologiczną.
Pierwotnie planowano, że LNP dyskretnie dostarczają sekwencje mRNA do komórek w celu wytworzenia białek kolców, a tym samym tworzą odporność na wirusa COVID-19.
Jednak wiele badań na myszach wykazało, że LNP, rzekomo nietoksyczne i bezpieczne, są w rzeczywistości wysoce zapalne.
Te nanocząsteczki są bardzo trwałe i mogą trwać od 20 do 30 dni w organizmie. Podczas gdy utrzymują się w organizmie, jest prawdopodobne, że będą nadal aktywować układ odpornościowy, prowadząc do wyczerpania odporności i braku reakcji.
Badanie Thomasa Jeffersona również podzieliło się podobnymi odkryciami. Naukowcy zbadali, w jaki sposób LNP wpływają na układ odpornościowy, wstrzykując myszom te same LNP, które są stosowane w szczepionkach Pfizera, a niektóre myszy były nawet podwójnie dawkowane.
Zapalenie i odpowiedzi immunologiczne u myszy nie są pewnymi oznakami, że to samo stanie się u ludzi. Niemniej jednak myszy od dawna są wykorzystywane do testowania bezpieczeństwa i skuteczności leków stosowanych u ludzi; oznaki problemów immunologicznych wskazują na możliwe zagrożenia dla zdrowia u ludzi.

Autorzy stwierdzili, że myszy, które otrzymały dwie dawki, miały zmniejszoną odpowiedź immunologiczną podczas drugiego wstrzyknięcia w porównaniu z myszami, które otrzymały tylko jedną dawkę.
"Platforma szczepionkowa mRNA-LNP (nanocząsteczki) indukuje długoterminowe nieoczekiwane zmiany immunologiczne wpływające zarówno na adaptacyjną odpowiedź immunologiczną, jak i heterologiczną ochronę przed infekcjami" - napisali autorzy.
Wstępna ekspozycja na nanocząstki mRNA zmniejsza liczbę wrodzonych komórek
Myszy, którym wstrzyknięto dwie dawki LNP, miały zmniejszoną liczbę wrodzonych komórek odpornościowych, komórek odpornościowych pierwszej odpowiedzi.
Autorzy chcieli dowiedzieć się, w jaki sposób LNP, powłoka, która owija się wokół mRNA, wpływa na myszy, wstrzykując im różne odmiany SNP.
Myszy podzielono na trzy grupy, wszystkie trzy grupy otrzymały dwa zastrzyki, choć o różnej zawartości.
W pierwszym wstrzyknięciu większości myszy podano wstrzyknięcie LNP. Połowa otrzymała LNP zawierające sekwencje mRNA, a druga połowa otrzymała puste LNP bez mRNA w środku.
Pozostałym myszom podano zastrzyk osolonej wody. Myszy te są używane jako punkt odniesienia do porównania, ponieważ zastrzyki z osolonej wody nie powinny wprowadzać żadnych zmian w organizmie.
Dwa tygodnie później wszystkim trzem grupom podano ten sam zastrzyk LNP zawierający sekwencje mRNA dla białka grypy (HA). Drugi zastrzyk pozwolił ich komórkom wytworzyć białka HA, co wywołało odpowiedź immunologiczną. Planowano, że ta odpowiedź immunologiczna uczyni myszy odpornymi na wirusa grypy.
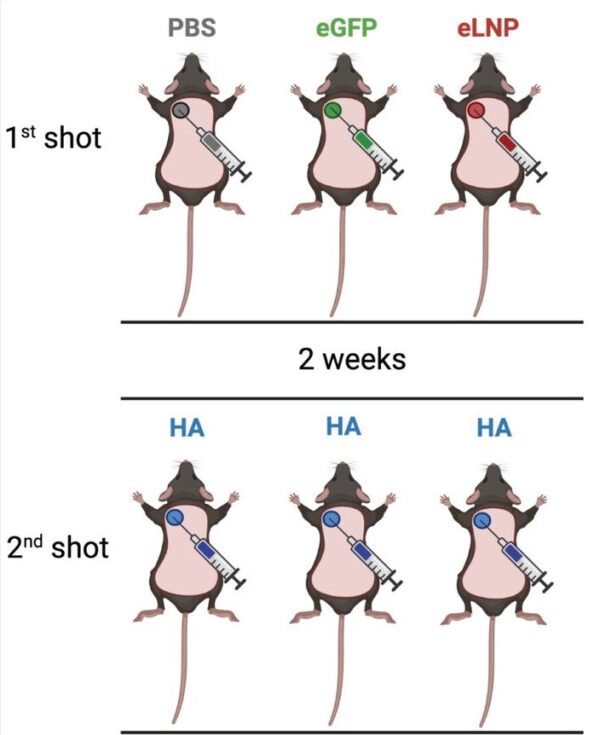
Naukowcy odkryli, że po drugim wstrzyknięciu wszystkie myszy rozwinęły obronę immunologiczną przed wirusem grypy.
Autorzy zaobserwowali, że myszy, którym podano dwie dawki LNP, były bardziej odporne na infekcję grypą, ponieważ straciły mniej na wadze. Co dziwne, te same myszy miały również niższą odpowiedź immunologiczną na szczepionkę przeciw grypie z mniejszą liczbą aktywowanych komórek odpornościowych.
Autorzy spekulowali, że ich "odporność" prawdopodobnie nie wynika ze wzmocnionej odporności, ale z produktu z alternatywnej ścieżki wyzwalanej przez LNP. Nie wiadomo, czy ta "oporność" będzie miała zastosowanie do innych zakażeń i może mieć zastosowanie tylko do grypy.
Wynika to z faktu, że badanie wykazało, że myszy, które były bardziej "odporne" na grypę, były w rzeczywistości bardziej podatne na infekcje grzybicze.
Naukowcy zainfekowali myszy Candida albicans, myszy, które otrzymały dwie dawki, straciły na wadze i miały gorszą kontrolę nad infekcją, co wskazuje na zmianę wrodzonej odpowiedzi immunologicznej.
Dalsze badania wykazały, że myszy te miały mniejszą liczbę neutrofili, które są najczęstszymi komórkami odpornościowymi pierwszej odpowiedzi.
Zadaniem neutrofili jest patrolowanie organizmu i atakowanie na oślep, gdy napotykają coś obcego, dlatego zmniejszona liczba neutrofili naraża osobę na większe ryzyko infekcji.
Ponieważ niekontrolowana infekcja grzybicza, szczególnie C. albicans, jest często oznaką osłabionej wrodzonej lub pierwszej odpowiedzi immunologicznej, autorzy podejrzewali, że zmniejszona liczba neutrofili mogła przyczynić się do wybuchu grzybów.
LNP powodują stan zapalny, a niektóre szlaki zapalne zmniejszają produkcję komórek krwi. Autorzy spekulowali, że dwie dawki LNP, które otrzymały niektóre myszy, mogły spowodować większy stan zapalny prowadzący do spadku produkcji krwinek i niskiej liczby neutrofili.
Chociaż są to spekulacje i nie jest pewne, czy skutki u myszy miałyby zastosowanie do ludzi, pojawiły się doniesienia u zaszczepionych osób o nagłym wystąpieniu ciężkiej niedokrwistości aplastycznej, stanu, w którym organizm nie może już wytwarzać wystarczającej liczby krwinek, szczególnie czerwonych krwinek.
Pojawiły się również doniesienia o osobach zaszczepionych COVID-19 rozwijających rzadkie choroby grzybowe i inne z pogorszeniem wcześniej istniejących chorób grzybiczych.
Chociaż poważna choroba grzybicza nie oznacza automatycznie słabego układu odpornościowego, niemniej jednak poważne infekcje grzybicze "występują najczęściej wśród osób ze słabym układem odpornościowym", pisze amerykańskie Centrum Kontroli i Zapobiegania Chorobom (CDC).
Liczba antygenów zmniejszona u myszy z wysoką ekspozycją na nanocząsteczki
W obrębie układu odpornościowego znajdują się pierwsi reagujący (wrodzone komórki odpornościowe) i drudzy odpowiedź (adaptacyjne komórki odpornościowe).
Pierwsi ratownicy przeprowadzają natychmiastowy atak po napotkaniu czegoś obcego. Jednak ich ataki są niespecyficzne i często nie mogą w pełni usunąć infekcji.
Dlatego adaptacyjne komórki odpornościowe, znane również jako limfocyty T i B, służą jako nasze drugie odpowiedzi.
Są one aktywowane około tygodnia po zakażeniu i usuwają infekcje poprzez narastanie silnych i specyficznych ataków.
Aby aktywować adaptacyjne komórki odpornościowe, limfocytom T i B należy przedstawić informacje na temat patogenu. W przypadku Sars-Cov-2 może to być fragment białka kolca.
APC (komórki prezentujące antygen), rodzaj pierwszej reagującej komórki, która przynosi kawałki wirusa, bakterii lub cząstek zakaźnych do adaptacyjnych komórek T lub B. Spowoduje to aktywację limfocytów T lub B, wywołując adaptacyjną odpowiedź immunologiczną.
Poniższy obrazek pokazuje komórkę dendrytyczną (APC), aktywującą limfocyt T poprzez przedstawienie mu antygenu, toksycznej lub obcej substancji.
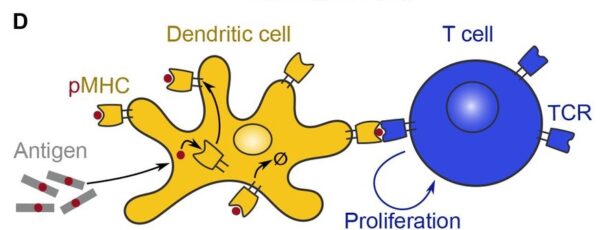
Jednak autorzy odkryli, że myszy, którym podano dwie dawki konwerterów mRNA, miały zmniejszoną prezentację antygenu w porównaniu z myszami, którym podano tylko jedną dawkę LNP.
Oznacza to, że mniej adaptacyjnych komórek odpornościowych zostało zmuszonych do aktywacji przeciwko białkom grypy.
Nanocząstki mRNA zmniejszają odpowiedzi limfocytów T i B
Autorzy stwierdzili, że myszy, które otrzymały dwa zastrzyki LNP, miały niższą odpowiedź limfocytów T i B na szczepionkę mRNA grypy niż myszy, którym podano tylko jedną dawkę.
Jako ostatnia linia odpowiedzi immunologicznej, limfocyty T i B mają kluczowe znaczenie dla zdolności naszego układu odpornościowego do usuwania infekcji.
Jednak u myszy, którym podano dwie dawki LNP, aktywowano mniej ich limfocytów T i B.
Grupy z podwójnymi dawkami miały również niższe stężenia przeciwciał (limfocyty B wytwarzają przeciwciała) przeciwko białku grypy.
Zmniejszona adaptacyjna odpowiedź immunologiczna była ogólnoustrojowa, utrzymująca się we wszystkich narządach i regionach. Jednak ta redukcja była jeszcze większa w miejscu wstrzyknięcia, zwłaszcza jeśli myszy otrzymały zastrzyki w tym samym miejscu dla obu strzałów, według autorów.
Z drugiej strony, grupa, której podano tylko jedno wstrzyknięcie LNP, miała wyższą odpowiedź limfocytów T i B z większą ilością wytwarzanych przeciwciał.
Autorzy stwierdzili, że ekspozycja na LNP zmniejszyła liczbę komórek progenitorowych T. Ponieważ komórki progenitorowe T dojrzewają do aktywowanych limfocytów T, mniej progenitorów oznacza zmniejszoną liczbę limfocytów T i odpowiedź.
Autorzy stwierdzili, że gdyby komórki progenitorowe T zostały usunięte przed szczepieniem, a następnie zwrócone po szczepieniu, aktywna liczba limfocytów T nie zostałaby zmniejszona. Sugeruje to, że LNP bezpośrednio zmniejsza liczbę komórek progenitorowych T, a tym samym zmniejsza odpowiedź limfocytów T.
"Wstępna ekspozycja na mRNA-LNP hamuje odpowiedzi limfocytów T" - napisali autorzy.
Ta obniżona odporność nie powinna być trwała, spekulowali autorzy.
Zauważyli, że odpowiedzi komórek B w większości ustępowały, jeśli wprowadzono odstęp 8 tygodni między pierwszą a drugą dawką.
Niemniej jednak autorzy nie zweryfikowali okresu potrzebnego do całkowitego wyzdrowienia, ani nie zweryfikowali, czy odpowiedź komórek B kiedykolwiek powróciła do zdrowia u myszy.
Jednak wstrzykiwanie myszom adiuwantów, takich jak sole glinu lub AddaVax, usunęło supresyjne działanie, jakie zastrzyki LNP miały na komórki odpornościowe myszy.
"Hamowanie adaptacyjnych odpowiedzi immunologicznych przez wstępną ekspozycję na mRNA-LNP jest długotrwałe, ale prawdopodobnie z czasem osłabnie."
Zmiany odporności z LNP mogą być dziedziczone
Jak wspomniano powyżej, myszy, którym wstrzyknięto dwie dawki LNP, były bardziej odporne na zakażenie grypą niż myszy, którym podano tylko jedną dawkę LNP.
Wykazano to poprzez doskonałe utrzymanie masy ciała myszy podczas infekcji, chociaż nie jest pewne, czy oporność pochodziła z odpowiedzi immunologicznej, czy z innego szlaku wywołanego przez LNP.
Co dziwne, ta zwiększona defensywność może zostać przekazana ich potomstwu. Dziedziczenie odporności na grypę jest silniejsze, jeśli oboje rodzice zostali zaszczepieni, a mniej, gdy tylko samotny rodzic, szczególnie jeśli tylko męski rodzic jest zaszczepiony.
Jednak badanie nie dotyczyło tego, czy potomstwo również dziedziczy osłabienie immunologiczne, takie jak spadek odporności na C. albicans, cechę obserwowaną również u myszy, którym podano dwie dawki LNP.
Implikacje badania i pilne pytania
Wyniki badania na myszach sugerują, że funkcje limfocytów T i B są tymczasowo zmniejszone u myszy i rodzą pytanie, czy to samo występuje u ludzi.
Adaptacyjna odpowiedź immunologiczna ma kluczowe znaczenie dla usuwania infekcji i zapobiegania chorobom przewlekłym, takim jak rak. Badanie sugeruje, że po dwóch szczepieniach lNP mRNA występuje kilka tygodni podatności myszy, co naraża je na większe ryzyko infekcji i raka.
Podobne doniesienia obserwuje się również u ludzi, chociaż nie ma jeszcze żadnych badań ustanawiających rozstrzygający związek.
Jednak zwiększona częstość występowania chorób zgłaszanych do Systemu Zgłaszania Niepożądanych Zdarzeń Szczepionkowych (VAERS) po szczepieniu COVID-19 sugeruje zmniejszoną odporność u osób po szczepieniu.
Pojawiło się wiele doniesień o nowotworach pojawiających się po szczepieniach przeciwko COVID-19.
W bazie danych VAERS zgłoszono 284 przypadki raka piersi po szczepieniu przeciwko COVID-19, podczas gdy w całej historii VAERS zgłoszono zaledwie 350 przypadków.
Po szczepieniu przeciwko COVID-19 zgłoszono 269 przypadków białaczki w porównaniu do 432 przypadków w całej historii VAERS.
Ponadto pojawiły się również doniesienia o nowych początkach i nawracających półpaścach po szczepieniach przeciwko COVID-19. Dane VAERS pokazują, że po szczepieniu przeciwko COVID-19 zgłoszono 7 559 przypadków półpaśca.
W całej historii VAERS zgłoszono 28 180 przypadków półpaśca po każdym szczepieniu, co oznacza, że około jedna czwarta przypadków półpaśca wystąpiła po szczepieniu przeciwko COVID-19.
CDC wskazało, że nowa diagnoza lub nawrót półpaśca występuje przede wszystkim u osób z upośledzonym układem odpornościowym i jest oznaką osłabionej odporności.
Chociaż badanie na myszach sugeruje możliwe implikacje zdrowotne u ludzi, nie wiadomo, czy wszystkie objawy i efekty obserwowane u myszy wystąpią u ludzi.
Niemniej jednak rosnące dane dotyczące zgłaszanych niepożądanych skutków zdrowotnych u ludzi po szczepieniu przeciwko COVID-19 uzasadniają dalsze badania. Konieczne jest również zbadanie nakładania się implikacji zdrowotnych dla myszy i ludzi.
"Biorąc pod uwagę szeroką ekspozycję dużej części populacji ludzkiej na szczepionki oparte na tej nowej technologii (mRNA), uzasadnione są dalsze badania, aby w pełni zrozumieć jej ogólne skutki immunologiczne i fizjologiczne. Określenie krótko- i długoterminowego wpływu tej platformy na zdrowie ludzkie pomogłoby zoptymalizować ją w celu zmniejszenia jej potencjalnie szkodliwych skutków "- podsumowali autorzy.
Przetlumaczono przez translator Google
zrodlo:https://www.theepochtimes.com/

Brak komentarzy:
Prześlij komentarz